유전자가위 치료제의 산업 구조 진화와 시장 성공 방정식
이정희 대표이사, ㈜디지털사이언스
1. 서론
유전자가위 기반 치료제(Gene Editing-based Therapeutics)는 질병의 근본 원인인 유전자 변이를 직접 교정함으로써 기존 치료 패러다임을 근본적으로 변화시키고 있는 차세대 치료 기술이다.
징크핑거 뉴클레아제(Zinc Finger Nuclease, ZFN)와 탈렌(Transcription Activator-Like Effector Nuclease, TALEN)을 거쳐 크리스퍼(Clustered Regularly Interspaced Short Palindromic Repeats, CRISPR)-Cas9 기술의 등장으로 유전자 편집의 효율성과 정밀성이 획기적으로 향상되었으며, 이를 기반으로 다양한 치료제가 임상 개발 및 상업화 단계에 빠르게 진입하고 있다.
현재 글로벌 유전자 편집 치료제 파이프라인은 총 360건을 훌쩍 넘겨, 전임상부터 승인 단계에 이르기까지 광범위한 개발이 진행되고 있다. 초기에는 겸상적혈구 빈혈(Sickle Cell Disease, SCD), 수혈의존성 베타 지중해성 빈혈(β-thalassemia, TDT)과 같은 희귀 혈액질환을 중심으로 개발이 진행되었으나 최근에는 종양, 감염병, 심혈관 및 대사 질환 등 다양한 적응증을 대상으로 확장되고 있다.
특히 최초의 CRISPR 기반 치료제인 카스게비(Casgevy)의 승인과 상업적 성과는 이 기술이 연구 단계를 넘어 실제 시장에서 작동하는 치료 플랫폼으로 자리 잡았음을 보여주는 중요한 전환점으로 평가된다.
반면 일부 치료제는 전달 효율, 안전성, 치료 지속성 문제로 인해 임상 개발이 중단되거나 전략이 수정되었으며, 이는 유전자 편집 원천기술 고도화에 더해 전달 기술과 편집 정확도 개선 등의 필요성을 강조한다.
이러한 흐름 속에서 유전자가위 기반 치료제 산업은 단순한 기술 혁신 단계를 넘어, 글로벌 파이프라인 확대와 적응증 확장이라는 ‘산업 구조의 진화’ 단계에 진입하고 있다. 동시에 전달 기술, 안전성, 비용, 규제 전략 등 상업화 성공을 좌우하는 다양한 요소들이 복합적으로 작용하며 산업의 방향성을 결정하고 있다.
2. 글로벌 파이프라인 현황 및 개발 단계 분석
유전자가위 기반 치료제 산업은 CRISPR-Cas9 기술의 임상 적용이 본격화되면서 연구 단계에서 상용화 단계로 빠르게 진입하고 있다. 현재 글로벌 유전자 편집 치료제 파이프라인은 후보물질 발굴(discovery) 및 전임상에서 승인 단계에서 전주기 개발 단계에 걸쳐 광범위하게 분포하고 있으며, 이는 해당 기술이 초기 연구 단계에서 실제 임상 치료 플랫폼으로 구조적으로 전환되었음을 의미한다.
전체 파이프라인은 360~400건 수준으로 2배 이상 증가했으며, 최초의 CRISPR 치료제인 Casgevy는 2025년 한 해 동안 약 1억 1,600만 달러의 매출을 기록하며 초기 상업화 가능성을 증명했다. Casgevy는 현재 초기 시장 진입 단계로 환자 접근성 확대와 함께 제조 인프라 및 치료센터 구축이 병행되고 있는 상황이다.
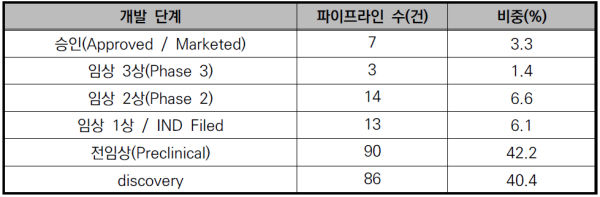
<표 1> 개발 단계에 따른 파이프라인 분포
출처: ClinicalTrials.gov, wikipedia, Google Scolar,U.S. SEC (http://www.sec.gov/) 등 다수 자료
<표 1>과 같이 전체 파이프라인 중 활성 상태인 213건을 분석한 결과, 현재 승인 단계(Approved / Marketed)에 도달한 치료제는 유전자를 삽입(addition)하는 방식을 포함하여 총 7건이다. 승인 사례는 아직 제한적이지만, 이는 유전자 편집 기술이 실험적 단계를 넘어 실제 의료 현장에서 활용되기 시작했음을 의미한다. 대표적으로 Casgevy는 SCD 및 TDT 치료제로 승인되며 유전자 편집 기반 치료의 임상적 실현 가능성을 입증한 역사적 전환점이 되었다.
활성 파이프라인 중 임상 단계(Phase 1~3) 후보물질은 총 30건으로 전체의 약 14.1%를 차지하고 있다. 특히 임상 2상의 비중이 상대적으로 높아 초기 임상에서 안전성을 입증한 후보물질들이 본격적인 효능 검증 단계로 순조롭게 진입하고 있음을 보여준다. 또한 혈액 질환을 넘어 종양, 감염병 등 다양한 질환 영역으로 적응증이 확장되고 있는 것도 중요한 특징이다.
초기 개발 단계(전임상 및 discovery) 비중은 80%를 상회하고 있으며, 이는 기존 CRISPR-Cas9의 한계를 보완할 수 있는 염기 교정(Base Editing) 및 프라임 교정(Prime Editing) 등 차세대 정밀 편집 기술 기반 연구가 확대되고 있기 때문으로 풀이된다.
이러한 대규모 초기 단계 파이프라인의 존재는 유전자 편집 치료제 분야가 지속적이고 안정적인 미래 성장 기반을 확보하고 있음을 강력히 시사한다.
유전자가위 치료제는 유전자 편집이 수행되는 위치에 따라 체외(ex vivo) 편집과 체내(in vivo) 편집으로 구분되며, 이는 치료 전략 및 적용 가능 질환 범위를 결정하는 핵심 요소이다.
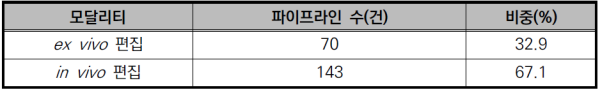
<표 2> 편집 방식에 따른 파이프라인 분류
최신 파이프라인을 편집 방식을 기준으로 분석한 결과, in vivo 편집이 67% 이상으로 증가하며 산업의 중심축 이동이 관찰되었다. 이는 아데노부속바이러스(Adeno Associated Virus, AAV) 및 지질 나노입자(Lipid Nano Particle, LNP) 기반 전달 기술 발전에 따른 것으로 여겨진다.
ex vivo 치료제는 환자의 조혈모세포, T 세포, NK 세포 등을 활용하여 체외에서 유전자 편집 후 환자에게 재투여하는 방식이다. 유전자 편집된 세포를 체내에 투여하기 전에 품질을 검증할 수 있어 높은 안전성과 정확도를 확보할 수 있다는 장점이 있으며 현재까지 가장 높은 임상 성공률을 보인다. 하지만 환자 맞춤형 제조 과정으로 인해 높은 제조 비용이 발생하고 질환 적응증의 확장에 있어 한계가 존재한다.
대표적인 예가 Vertex Therapeutics 및 CRISPR Therapeutics에서 공동개발해 승인된 Casgevy이다. Casgevy는 환자의 조혈모세포 내 BCL11A 유전자를 편집해 태아형 헤모글로빈(HbF)을 재활성화시켜, 단회 투여(one-time treatment)만으로 SCD 및 TDT를 치료한다.
in vivo 치료제는 전달체를 이용하여 체내에서 직접 유전자 편집을 수행하는 방식으로, 전달 기술의 발전과 함께 가장 빠르게 성장하고 있는 분야다. 최신 파이프라인 분석 결과, in vivo 치료제 비중이 67.1%를 차지하며 향후 유전자 편집 치료제 산업 성장을 주도할 핵심 기술로 자리매김했다.
대표적인 in vivo 치료제는 Intellia Therapeutics의 ATTR 아밀로이드증 치료제 후보물질 ‘NTLA-2001’이다. 현재 NTLA-2001은 임상1/2상 및 확장 연구 단계에서 간세포를 표적한 LNP 기반 유전자 편집 전략의 유효성과 안전성을 입증하고 있으며, 일부 적응증에서 후기 임상 진입을 위한 기반을 확보하고 있다.
또다른 전달 기술은 AAV 기반 접근법이다. Excision BioTherapeutics의 ‘EBT-101’은 HIV 바이러스 DNA 제거를 목표로 임상 1/2상을 진행하며 in vivo 편집 기술의 가능성을 넓히고 있다.
in vivo 편집 방식은 제조 공정 단순화, 다양한 조직 적용 가능성, 대량 생산 측면에서 상업화에 유리한 구조를 가진다. 이러한 강점을 바탕으로 감염병, 심혈관 및 대사 질환 등으로 적용 영역을 급격히 확장하고 있다.
현재 유전자가위 기반 치료제 산업은 초기 상용화 단계를 넘어 본격적인 성장 국면에 접어들고 있다. 산업의 중심은 ex vivo 방식에서 in vivo 방식으로 이동하고 있으며, 이는 AAV 및 LNP 등 전달 기술과 Base Editing, Prime Editing 등 차세대 플랫폼 기술의 결합에 따른 구조적 변화이다. 이러한 전환은 유전자 편집 기술이 특정 질환을 넘어 다양한 질환에 적용 가능한 범용 치료 플랫폼으로 진화하고 있음을 시사한다.
3. 질환별 적응증 현황 및 미충족 수요
유전자가위 기반 치료제는 질병의 근본 원인인 유전적 결함을 직접 교정할 수 있는 기술로, 기존 치료법이 해결하지 못했던 미충족 의료 수요(unmet medical needs)를 해결할 수 있는 새로운 치료 패러다임으로 자리 잡고 있다.
초기에는 단일 유전자 변이에 의해 발생하는 희귀 혈액 질환을 중심으로 개발이 진행되었으나 현재는 종양, 감염병, 신경계 질환 및 심혈관 대사 질환 등으로 급속히 확장되고 있다.
특히 기존 치료법이 질병 진행을 억제하는 수준에 머물렀던 것과 달리, 유전자 편집 치료제는 질병의 원인을 직접 제거하거나 교정함으로써 단회 투여로 장기적 또는 잠재적으로 지속적인 치료 효과를 기대할 수 있다는 점에서 근본적 치료 전략으로 평가된다.
현재 글로벌 유전자가위 기반 치료제 파이프라인은 총 362건으로 조사되었으며, 이 중 활발히 개발되고 있는 활성 파이프라인(213건)을 적응증 기준으로 분류한 결과는 <표 3>과 같다.
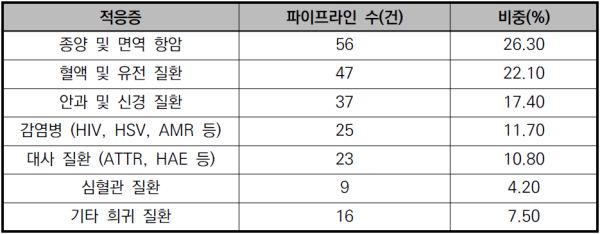
<표 3> 적응증별 파이프라인 분포 현황
적응증별 파이프라인 분포 현황을 보면, 현재의 유전자가위 기술은 희귀 혈액 질환 중심으로 검증이 이루어지던 초기 단계를 넘어 종양학, 신경계, 만성 질환 등 대형 적응증으로 확장되는 '기술 확산 및 상용화 초기 정착 단계'에 진입한 것으로 분석된다.
우선 종양 및 면역 항암 분야는 혈액 질환을 역전하며 가장 큰 비중(26.3%)으로 시장 성장을 주도하고 있으며 유전자 편집을 통해 기능을 강화한 CAR-T(Chimeric Antigen Receptor T-cell) 및 T 세포 치료제가 핵심 전략으로 활용되고 있다. 면역 세포의 특정 유전자를 편집해 암세포의 면역 회피를 차단하고 공격 능력을 극대화하는 방식으로, 최근 자가(autologous) 세포 치료의 한계를 극복하기 위한 동종(allogenic) 세포 치료 개발로의 흐름이 뚜렷이 관찰되고 있다.
특히 건강한 공여자의 T세포를 사용한 ‘기성품(off-the-shelf)’ 방식 치료제인 ‘CTX110(CRISPR Therapeutics)’, ‘BEAM-201(Beam Therapeutics)’ 및 ‘CB-010(Caribou Biosciences)’ 등이 자가 세포 치료의 한계를 극복하기 위해 적극적으로 개발되고 있다.
혈액 및 유전 질환은 임상적 성공과 승인을 가장 먼저 달성한 영역이다. 대부분 발병 원인은 단일 유전자 변이이므로 유전자 교정 효과가 명확하게 나타나며 기술 검증에도 가장 적합한 것으로 여겨지고 있다. 첫 유전자 편집 치료제인 Casgevy 역시 혈액 질환을 대상으로 초기 상업화 가능성을 입증했다. 최근에는 알파-1 항트립신 결핍증(AATD), 혈우병, 근이영양증 등으로 파이프라인이 정교하게 확장되고 있다.
안과 및 신경 질환은 전달 기술(AAV, LNP)의 정밀도 향상으로 가장 가파르게 성장해 17.4% 비중을 차지하고 있다. 레베르 선천성 흑암시(Leber Congenital Amaurosis Type 10, LCA10), 레베르 유전성 시신경병증(Leber Hereditary Optic Neuropathy, LHON), 망막색소변성증(Retinitis Pigmentosa, RP) 등의 안과 질환과 파킨슨병, 다계통위축증(Multiple System Atrophy, MSA) 등 중추신경계 질환 파이프라인이 대거 유입되었다. 이는 유전자 편집 기술이 미세한 조직 내 세포까지 정밀하게 타깃할 수 있는 수준으로 진화했음을 보여준다.
감염병 분야 역시 HIV(Human Immunodeficiency Virus) 및 차세대 항생제 내성(Antimicrobial Resistance, AMR) 연구를 중심으로 꾸준히 확장되고 있다. 기존 감염병 치료는 바이러스 증식 억제에 그쳤으나 지금은 바이러스 DNA 자체를 제거하는 근본적 완치를 목표로 한다. ‘EBT-101’은 HIV 프로바이러스 DNA를 제거하는 전략으로 임상1/2상을 진행 중이며, ‘BD-111(BDGene)’은 HSV-1(Herpes Simplex Virus-1) 잠복 바이러스 제거를 목표로 임상2상 단계에 있다.
또한, CRISPR 기반 박테리오파지(crPhage) 기술을 활용하여 특정 병원성 세균만 선택적으로 제거하는 치료기술도 연구되고 있으나 전반적으로는 아직 초기 연구 및 전임상 단계가 대부분이다. 혈액암 환자의 대장균(E.coli) 감염증 치료제 ‘SNIPR-001(SNIPR Biome)’는 최근 임상1상을 완료했으며, 재발성 요로감염(uncomplicated Urinary Tract Infection, uUTI) 치료제 ‘LBP-EC01(Locus Biosciences)’는 임상2상 단계에서 효능 검증 중이다.
대사 및 심혈관 질환 등 대중적 질환은 in vivo 편집 기술과 LNP 전달체의 결합이 가장 활발히 적용되고 있는 영역이다. 환자군이 매우 방대하여 향후 유전자가위 치료제 시장에서 가장 큰 상업적 폭발력을 가질 것으로 전망되고 있다.
ATTR 아밀로이드증 치료제 ‘NTLA-2001’은 임상 1/2상 및 확장 연구를 통해 강력한 TTR(transthyretin) 감소 효과를 입증하며 후기 임상 진입 가능성을 높이고 있다. 고콜레스테롤혈증 등 심혈관 질환을 대상으로 개발 중인 ‘VERVE-101(Verve Therapeutics)’은 임상1b상에서 안전성 이슈로 일시적 임상 보류(clinical hold) 후 ‘VERVE-102’로 전략을 고도화하며 대중적 만성 질환에 대한 in vivo 편집의 가능성을 타진하고 있다.
현재 유전자가위 기반 치료제 파이프라인 구조는 다음과 같은 3단계의 진화 과정을 명확히 보여주고 있다.
<1단계> 희귀 혈액 질환 중심의 기술적 실현 가능성 검증 (Proof of Concept)
· 단일 유전자 표적 및 ex vivo 편집: 유전적 원인이 명확하고 체외 편집 후 재주입이 용이한 혈액 질환을 중심으로 유전자가위의 정밀성과 안전성 검증
· 임상 적용 가능성 최초 확립: ex vivo 접근법을 통해 실제 환자에서의 유의미한 치료 효과를 입증하며 유전자 편집의 임상적 실현 가능성 공식화
· 완치 패러다임 상징: Casgevy 승인을 통해 유전자 편집이 난치병을 근본적으로 해결하는 표준 치료 도구임을 입증
<2단계> 종양 및 감염병으로의 적용 영역 확대 및 고도화 (Expansion & Precision)
· 복합 질환 메커니즘 대응 및 기술 고도화: 복잡한 면역 체계 조절이 필요한 암이나 세포 핵 내의 잠복 바이러스 제거를 위한 정밀 편집 기술 임상 본격화
· 적응증 확장과 임상적 유효성 검증: 희귀 질환에서 종양학 및 감염병 분야로 적응증을 확장하며 실질적 치료 효능과 유전자 편집 플랫폼의 범용성 검증
· 동종 제제 전환 및 상업적 범용성 확보: 환자 자가 제제의 한계를 넘어 ‘기성품’ 방식 동종 치료제 개발로 제조 원가 절감 및 상업적 대중화 동시 추구
<3단계> 심혈관, 대사, 신경계 등 만성 및 대중적 질환으로의 범용 플랫폼 확장 (Universal Platform)
· in vivo 편집 및 차세대 전달 기술의 결합: AAV 및 LNP 등 전달 플랫폼 혁신을 바탕으로, 체내에서 직접 교정하는 방식으로 패러다임 전환
· 대규모 환자군 및 만성 질환 대응: 고혈압, 고콜레스테롤혈증 등 만성 질환으로 적응증을 확장하며 단회 투여로 평생 약물 복용을 대체하는 '백신형 치료제'로서의 가능성 제시
· 표준 치료 옵션 편입: 유전자가위 기술이 특정 난치병 치료를 넘어 대중적 질환의 근본 원인을 해결하는 범용 치료 플랫폼으로 진화하며 핵심 표준 치료 체계로 안착
유전자가위 기술은 기존 의학이 도달하지 못했던 '근본 원인 제거'라는 혁신적 접근을 통해 난치성 암 및 완치가 불가능했던 만성 감염, 항생제 내성균 등 미충족 의료 수요를 해결하는 차세대 표준 치료(Standard of Care) 플랫폼으로 빠르게 자리 잡고 있다.
4. 규제 지정 및 상업화 성공 전략
유전자가위 기반 치료제는 기존 치료법으로 해결이 어려운 희귀 및 난치성 질환을 주요 타깃으로 하기 때문에, 상업화 성공을 위해서는 규제기관의 신속 승인 프로그램(Regulatory Expedited Programs) 활용을 핵심 전략으로 삼아야 한다. 미국 FDA와 유럽 EMA는 혁신 치료제의 조기 공급을 위해 다양한 프로그램을 운영 중이며 유전자 편집 치료제는 이러한 제도의 최대 수혜 분야라 할 수 있다.
주요 규제 지정 프로그램으로는 패스트트랙 지정(Fast Track Designation, FTD), 혁신의약품 지정(Breakthrough Therapy Designation, BTD), 가속승인(Accelerated Approval), 희귀의약품 지정(Orphan Drug Designation, ODD), 첨단재생의료치료제(Regenerative Medicine Advanced Therapy, RMAT) 지정, 소아희귀의약품 지정(Rare Pediatric Disease Designation, RPDD) 등이 있다.
FTD는 심각하거나 생명을 위협하는 질환을 대상으로 하며, 기존 치료법 대비 명확한 치료 개선 가능성이 있는 경우 부여된다. FTD를 획득하면 FDA와 수시로 긴밀한 협의를 진행하고 단계별 자료 제출이 가능한 롤링 리뷰(rolling review)를 통해 심사 준비 및 대응 기간을 획기적으로 단축할 수 있다.
가속승인은 임상적 유효성을 직접 입증하는 대신 질병 진행을 예측할 수 있는 대체 평가변수(surrogate endpoint)를 기반으로 조기 승인하는 제도이다. 유전자 편집 치료제 분야에서 사용되는 대체 평가변수는 특정 단백질 발현량 감소, 유전자 교정 효율, 바이러스 DNA 제거 수준, 특정 바이오마커 변화 등이 있다. 가속승인 이후에는 확증 임상(confirmatory trial)을 통해 임상적 이점을 입증해야 하지만, 최종 결과 도출 전 시장 선점과 대규모 투자 유치를 가능케 하는 강력한 상업적 레버리지가 된다.
ODD는 환자 수가 적은 희귀질환 치료제 개발을 장려하기 위한 제도이다. 특히 유전자가위 치료제의 주요 적응증인 SCD, TDT, 뒤센근이영양증(Duchenne Muscular Dystrophy, DMD), ATTR 아밀로이드증 등은 대부분 희귀질환이므로 사실상 상업화 성공 확률을 높일 수 있는 필수적인 규제 전략이다.
ODD 제품은 승인 후 시장 독점권(미국 7년, 유럽 10년)을 확보하여 경쟁 제품의 진입을 원천 차단하고 고가 약가(premium pricing) 전략을 유지할 수 있다. 그밖에도 임상 비용 최대 25% 세액 공제, FDA 허가 심사비(user fee) 면제 등의 혜택이 주어진다.
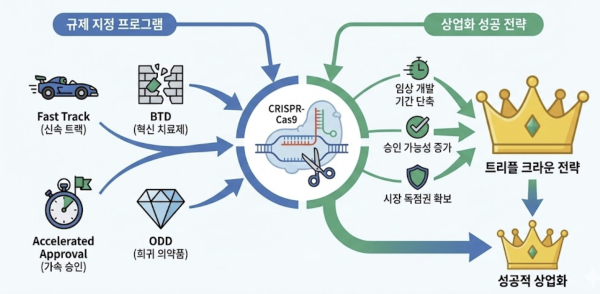
유전자가위 치료제의 상업적 성공의 핵심은 이른바 '트리플 크라운(Triple Crown)' 전략이다. 트리플 크라운이란 신속 개발 지정(FTD, BTD, RMAT)으로 개발 속도를 높이고, 가속승인으로 시장 진입 시점을 앞당기며, ODD로 독점적 수익 구조를 완성하는 통합 규제 전략을 의미한다.
다수 유전자가위 치료제 개발 기업들은 임상 개발 초기 단계부터 규제기관과 긴밀한 협의를 통해 다양한 신속 승인 프로그램을 확보하는 전략을 구사하고 있다. 이러한 규제 지정은 단순한 행정적 혜택을 넘어 임상 개발 성공률과 상업화 가능성을 크게 높이는 핵심 요소이기 때문이다.
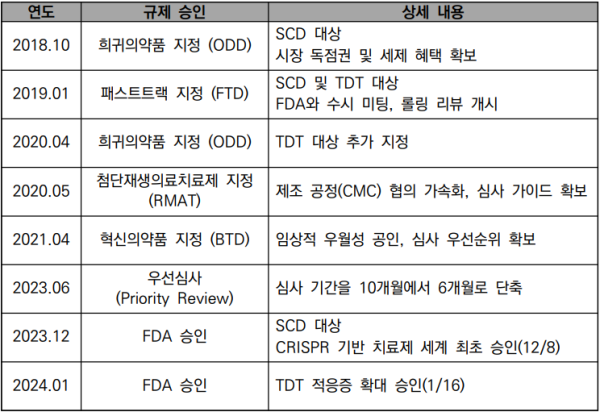
Casgevy는 실제로 <표 4>와 같이 ODD, FTD, RMAT, BTD 등을 모두 확보해 시장에 안착한 대표적 성공 사례다.
<표 4> ‘Casgevy’ FDA 규제 지정 타임라인
그 밖에 TDT 치료제 ‘진테글로(Zynteglo, Bluebird Bio)’와 SCD 치료제 ‘리프제니아(Lyfgenia, Bluebird Bio)’ 및 DMD 치료제 ‘엘리비디스(Elevidys, Sarepta Therapeutics)’ 역시 트리플 크라운 전략이 제대로 주효한 제품이다.
Zynteglo와 Lyfgenia는 동일한 렌티바이러스 벡터 플랫폼을 적응증별로 이원화하여 각각 2013년 및 2014년부터 ODD, FTD, BTD 및 RMAT 지정 후 우선심사(Priority Review)를 거쳐 2022년 및 2023년에 최종 승인되었다.
Elevidys는 가속승인을 통해 조기승인된 대표적 사례로, 2020년 ODD 및 RPDD를 시작으로, 가속승인, 우선심사를 거쳐 2024년 6월 최종 승인 및 적응증도 확대되었다. 가속승인을 통해 1년 먼저 시장에 진입한 후 적응증을 확대해, 규제기관의 신속심사 프로그램이 유전자 치료제의 상업화에 결정적인 역할을 한다는 것을 보여준다.
Bluebird Bio와 Sarepta는 당시에 획득한 우선심사 바우처(Priority Review Voucher, PRV)를 각각 1억 달러 내외의 현금으로 빅파마에 매각하며 주식가치 희석 없는 재무적 가치를 창출하기도 하였다.
최근 후기 임상에 진입한 NTLA-2001과 NTLA-2002 역시 이러한 규제 혜택을 적극활용하여 조기 상업화를 추진하고 있다.
5. 임상 시험의 주요 성과와 실패 사례 분석
유전자가위 기반 치료제는 기존 치료법으로 해결할 수 없었던 난치성 유전 질환, 만성 감염병, 종양 등을 근본적으로 치료할 수 있는 혁신적 플랫폼으로 평가받는다. 그러나 임상 개발 과정에서는 전달 효율, 표적 외 편집(off-target), 치료 효과의 지속성 등 복잡한 과제가 존재한다.
현재까지 보고된 임상 시험의 성공 및 실패 사례는 향후 기술 진화 방향과 상업화 전략 수립에 결정적인 시사점을 제공한다. 일부 치료제는 매우 높은 치료 효과를 입증하며 상업화에 성공한 반면, 일부는 효과 부족, 안전성 문제, 전략적 개발 방향 전환 등의 이유로 임상이 중단되거나 수정된 사례도 보고되고 있다.
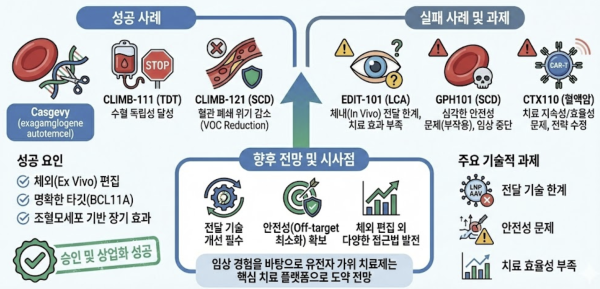
<그림 2> 성공 / 실패 요인 분석을 통해 도출된 주요 기술적 과제
Casgevy는 CRISPR-Cas9 기반 치료제 중 최초로 임상3상 성공 및 승인에 도달하며 새로운 유전자 편집 시대를 열었다. Casgevy의 임상 성공 요인은 명확한 단일 유전자 타깃(BCL11A 변이), 고정밀 ex vivo 편집, 조혈모세포 기반 장기 지속 효과 등을 들 수 있다.
Casgevy 승인은 2건의 임상3상 결과를 근거로 이루어졌다. SCD 대상 ‘CLIMB-121’ 임상의 평가변수는 혈관폐쇄위기(Vaso-Occlusive Crises, VOC) 감소율이었으며 대다수 환자에서 VOC가 완전히 소실되거나 현저히 감소하였다. TDT 임상 ‘CLIMB-111’의 평가변수는 수혈 독립성이었으며 대부분의 환자가 장기간 수혈 없이 정상적인 헤모글로빈 수준을 유지하는 결과를 보였다.
임상을 통해 SCD 및 TDT의 원인 유전자 BCL11A 조절을 통한 HbF 재활성화라는 Casgevy의 기전의 유효성을 확인함으로써 유전자 편집 치료가 단순한 증상 개선을 넘어 질병의 병태생리적 원인을 직접 교정할 수 있는 전략임을 알 수 있다.
하지만 임상 개발 과정에서는 치료 효과 부족, 안전성 문제, 또는 전략적 방향 전환 등의 이유로 개발이 중단되거나 수정되는 등 기술적 한계를 명확히 보여주는 실패 사례도 존재한다.
LCA 치료를 위한 in vivo 치료제 EDIT-101은 망막 세포의 문제 유전자를 직접 교정하는 전략을 적용하였다. 그러나 실제 임상에서는 반응률이 기대에 미치지 못하는 등 일관된 임상적 유의성을 확보하지 못하며 현재 전략적 보류(strategic pivot) 상태이다. 연구진은 이러한 제한적인 치료 효과의 이유로 타깃 조직인 망막까지의 전달 효율 및 조직 특이적 편집 효율 저하를 꼽았다.
EDIT-101은 임상에 진입한 최초의 in vivo CRISPR 치료제로 큰 기대를 모았음에도 불구하고 전달 기술의 부재로 인해 일관된 치료 효과를 확보하지 못해 결국 전략적 우선순위에서 배제된 사례이다.
SCD 치료제 ‘GPH101(Graphite Bio)’은 임상 중 일부 환자에서 심각한 혈액학적 부작용이 발생하며 개발이 중단되었다. 이는 의도하지 않은 유전자 교정, 세포 기능 이상, 세포 생존율 감소 등 안전성 검증이 상업화의 가장 높은 허들임을 보여준다.
혈액암 치료제 ‘CTX110(CRISPR Therapeutics)’는 CAR-T 치료제로, 초기 임상에서는 일부 치료 효과가 확인되었으나 반응 지속성 문제로 인해 현재는 공정 효율을 개선한 차세대 후보물질 CTX112로 개발 전략이 수정되었다. 치료 지속성, 면역 회피, 세포 생존율 유지 등이 유전자 편집 기반 세포치료 개발에 있어 중요한 고려사항이 되어야 하는 이유다.
결국 유전자가위 기반 치료제의 임상 개발에 있어 가장 중요한 병목 구간은 전달 기술과 안전성이다.
유전자 편집 시스템을 체내로 전달하는 기술은 치료 효능을 좌우하는 핵심 요소지만 현재 주로 사용되는 AAV 및 LNP는 여전히 한계가 존재한다. 대표적으로 면역 반응 유발, 간 독성, 조직 특이성 제한 등의 문제가 보고되고 있으며 이러한 한계점은 특히 in vivo 치료제에서 임상적 유효성 확보를 어렵게 만드는 주요인으로 작용한다.
안전성 측면에서 가장 중요한 리스크는 표적이 아닌 유전자를 편집해 버리는 오프타겟(off-target)이다. 오프타겟은 정상 유전자 손상, 세포 기능 이상, 종양 발생 가능성까지 초래할 수 있어 임상 적용의 가장 큰 걸림돌이다.
따라서 고정밀 편집기술 개발과 함께 오프타겟 최소화 전략 역시 유전자 편집 치료제의 상용화를 위한 필수 조건이라 할 수 있다.
in vivo 편집의 경우, 표적 조직 및 세포에서 충분한 편집 효율을 확인하기는 기술적으로 어렵다. 편집 효율이 낮으면 치료 효과가 제한적이며 자연스레 임상적 유의성도 확보하기 어려워진다.
유전자가위 기반 치료제의 임상 성패 사례를 종합하면 다음과 같은 시사점을 도출할 수 있다.
(1) 현재까지는 ex vivo 편집 방식이 가장 높은 임상 성공률을 보이고 있으며 기술적 안전성이 입증된 방식이다.
(2) 질환의 병태생리를 감안한 적절한 타깃 선택이 임상 성공률을 결정짓는 중요한요인이다.
(3) 전달 기술의 고도화는 향후 in vivo 치료제의 임상 성공을 좌우할 핵심 변수이다.
(4) 안전성 확보는 임상 성공 뿐 아니라 규제 승인 및 상업화의 필수 전제 조건이다.
6. 향후 과제와 미래 전망
유전자가위 기반 치료제는 질병의 증상 완화를 넘어 근본적 치료(curative therapy)를 구현하는 새로운 패러다임으로 자리 잡고 있다. 현재 글로벌 파이프라인은 희귀 혈액질환을 넘어 다양한 질환 영역으로 확장되고 있으나, 보편적으로 확산되기 위해서는 여전히 기술적·상업적 과제가 존재한다.
유전자가위 기반 치료제의 상업적 확산을 위해서는 전달 효율과 안전성 확보가 핵심 기술 과제로 작용한다. 현재의 AAV, LNP 기반 전달체는 간 조직 중심으로는 유효성이 입증되었으나, 다양한 조직으로의 확장에는 여전히 한계가 존재한다. 오프타겟에 따른 안전성 문제 또한 임상 적용의 주요 리스크가 되고 있다.
결과적으로 전달 기술과 편집 정확도는 향후 임상 성공률과 적응증 확장을 좌우하는 핵심 변수로 작용할 것이다.
상업화 측면에서는 높은 치료 비용이 유전자 편집 치료제 확산의 가장 큰 제약 요인으로 평가된다. 현재 치료제는 복잡한 제조 공정과 환자 맞춤형 ex vivo 편집, 높은 기술 난이도 및 제한된 환자 수로 인해 높은 가격이 형성되어 있으며, 이는 치료 접근성을 제한하고 의료 형평성 문제를 야기할 수 있다.
이러한 한계를 극복하기 위해서는 ex vivo 중심의 치료 구조에서 in vivo 방식으로의 전환, 제조 공정의 단순화 및 대량 생산 기술 확보, 그리고 보험 및 공공 의료 시스템과의 연계가 중요하다. 비용 절감과 접근성 개선은 향후 유전자 편집 치료제가 대중적 치료 옵션으로 자리 잡기 위한 핵심 요소가 될 것이다.
유전자 편집 기술은 유전자 정보 활용과 관련된 윤리적·사회적 문제를 수반한다. 환자 유전자 정보 보호, 치료 접근의 공정성, 기술 남용 가능성 등은 지속적으로 관리되어야 할 중요한 이슈이며, 기술 발전과 병행한 규제 체계 정비와 사회적 합의 형성이 필수적이다.
CRISPR-Cas9이 시장의 문을 열었다면, 향후에는 DNA 절단 없이 염기를 교정하는 Base Editing이나 정밀도를 극대화한 Prime Editing 등이 차세대 핵심 기술로 자리 잡을 것이다.
적용 질환 영역 또한 초기 희귀 혈액질환에서 종양, 감염병, 심혈관 및 대사 질환을 넘어 머잖은 미래에는 신경계 및 자가면역 질환의 적응증 확장이 본격화되고 있다.
종합적으로, 유전자가위 치료제는 규제 전략의 정교화와 전달 기술의 고도화를 통해 정밀의학의 핵심축으로 안착할 전망이다. 특히 차세대 편집기술과 비바이러스 전달 시스템의 결합은 치료의 안전성과 경제성을 동시에 향상시켜 보편적 치료 옵션으로의 전환을 가속화 할 것으로 기대된다.
* 본 기고문은 과학기술정보통신부에서 시행한 「유전자편집·제어·복원기반기술개발사업」수행의 일환으로 작성되었습니다.
* 본 내용은 유전체편집연구지원사무국(GERC)의 의견과 다를 수 있음을 밝힙니다.
* 인용, 발표하실 때에는 반드시 출처를 밝혀주시기 바랍니다.